



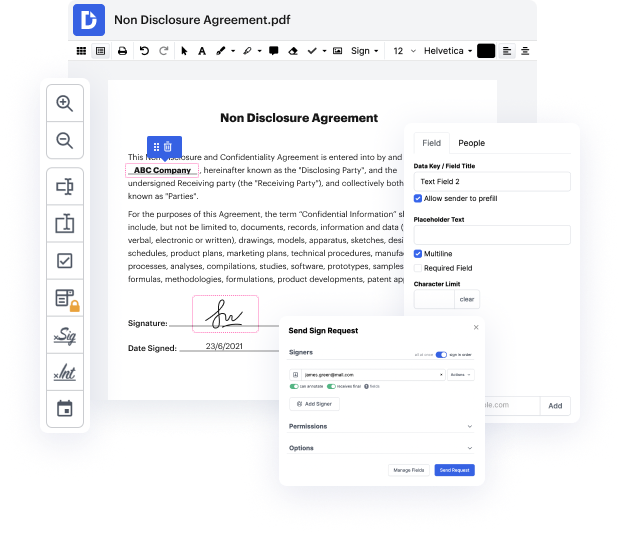
COVID cambió para siempre cómo las organizaciones ven sus protocolos y procedimientos internos. Influyó en organizaciones de todos los tamaños y sectores, planteando nuevos desafíos para mantenerse conectados. La pandemia indicó que todas las organizaciones deberían incorporar herramientas digitales en sus rutinas diarias. Se volvieron esenciales para mucho más que los modelos de trabajo híbrido.
Aplicaciones como DocHub te permiten mejorar tu administración de archivos y procesos de aprobación. DocHub es tu herramienta de referencia para la edición y firmas en línea de principio a fin. Facilita tus tareas diarias de generación y aprobación de contratos y acuerdos. Obtén acceso a Aplicación PDF para Fabricantes de Dispositivos Médicos | Solución de Gestión de Documentos para Fabricantes de Dispositivos Médicos características de edición superiores que cubren todas tus necesidades administrativas. Maneja cualquier tipo y formato de archivo, crea campos rellenables y recopila firmas de manera eficiente de tus colegas y clientes. No se requiere formación o experiencia previa.
Con Aplicación PDF para Fabricantes de Dispositivos Médicos | Solución de Gestión de Documentos para Fabricantes de Dispositivos Médicos, es posible optimizar la calidad de tus documentos, aumentar el proceso de aprobación y almacenar documentos completos de forma segura. Obtén un perfil gratuito de DocHub hoy y cambia tu suscripción cuando lo desees.
En este video, Peter Sibelius de medicaladvicehq.com proporciona una visión general de los requisitos de documentación para proyectos de desarrollo de dispositivos médicos. Él enfatiza la importancia de entender cómo todo encaja y ofrece una explicación simplificada del proceso. El objetivo es ayudar a los espectadores a ver el panorama general y obtener claridad sobre los entregables documentales típicos necesarios para tales proyectos. Recuerde que las situaciones individuales pueden variar, por lo que la información proporcionada es una visión general. Suscríbase para más contenido y consulte el curso en línea sobre control de diseño para dispositivos médicos.
En DocHub, la seguridad de tus datos es nuestra prioridad. Seguimos HIPAA, SOC2, GDPR y otros estándares, para que puedas trabajar en tus documentos con confianza.
Aprende más



